摩尔电导率moer diandaolu
相距1 m的两个平行板电极之间含有1 mol电解质的溶液时所具有的电导率称为摩尔电导率,用符号表示。由于电解质的量规定为1 mol,因此电极的面积或导电溶液的体积是随溶液浓度不同而改变的。若某电解质溶液的浓度为c(mol·m-3),则含有1 mol该电解质溶液的体积:
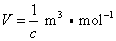
而电导率k的定义为两平行电极间距离为1 m时,1m3溶液的电导(即单位长度、单位横截面积物体的电导),故可得摩尔电导率与电导率k的关系:к
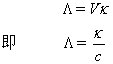
的单位是S·m2·mol-1。表示电解质的摩尔电导率时,应标明基本单元的化学式,例如,
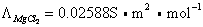
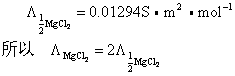
电解质溶液的摩尔电导率与浓度有关 (见下图)。强、弱电解质溶液的摩尔电导率总是随着浓度的减小而增大。对强电解质而言,在溶液中处于完全电离状态,浓度减小时,离子间作用力略有减弱,离子迁移速度略有增大,摩尔电导率稍有增大,曲线的
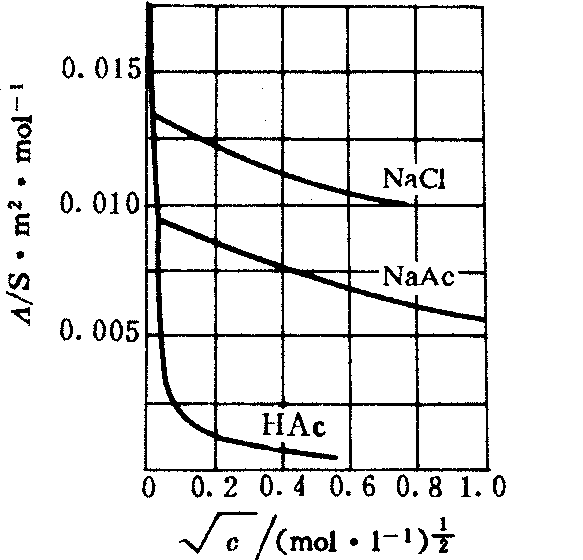
摩尔电导率与浓度的关系
延长线比较平缓地趋向于一极限值——无限稀释时的摩尔电导率°(注意°不是纯溶剂的),在浓度较低时 (小于0.01 mol·L-1),强电解质的摩尔电导率较好地遵守下列经验关系式: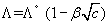
式中β为常数,c为浓度,将A对
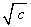 作图,得一直线,外推至与纵轴相交,所得截距即为°。
作图,得一直线,外推至与纵轴相交,所得截距即为°。对弱电解质来说,溶液稀释时,虽然电极间的电解质含量没有变,仍然是1mol,但电离度迅速增大,离子数目急骤增加,摩尔电导率显著上升,尤其在低浓度时,曲线上升的趋势更为陡峭,其延长线无法准确与纵轴相交。因此难于用作图法求得弱电解质无限稀释时的摩尔电导率°,用离子独立运动定律,可求得弱电解质无限稀释时的摩尔电导率。25℃时一些电解质的摩尔电导率见下表。