电导率diandaolu
物体的电导与其几何形状密切相关,若不说明几何形状及大小,比较两种不同物体的电导,不能真实反映两者导电能力的差异。性质均匀的物体,横截面积越大,电导值越大; 长度越长,电导值越小,即
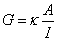
式中G为电导,A为横截面积,l为长度,к为比例系数,是单位长度、单位横截面积物体的电导,称为电导率,单位为S·m-1。它是个真正反映物体导电能力的物理量。电导率可直观地比较各种溶液的导电能力,不用考虑电极面积和电极间的距离等。例如,5%NH4Cl 溶液 k=9.180,10%NH4Cl 溶液k=17.78S·m-1,因此后者导电性比前者好。而电导G的数值不仅与浓度有关,还与电极面积、电极间距离等因素有关,因此不能简单地用电导值比较导电能力的强弱。
电解质溶液的电导率与溶液的浓度有关,如下图所示。对强电解质而言,浓度较小时,电导率随浓度增加很快增大,这是由于浓度增大,离子数目增多之故。当浓度增大到某一数值后,电导率反而减小,这是由于溶液中离子数目相当大,正、负离子间引力加大,使离子的迁移速度减慢,导致离子导电能力降低。对弱电解质而言,浓度加大时电离度减小,离子数增加得并不显著,因此电导率随浓度的变化
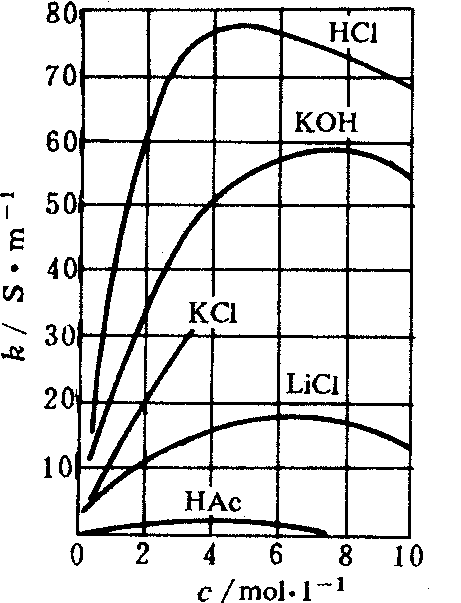
电导率与浓度的关系
不象强电解质那样明显。
电导率diandaolu
电阻率的倒数,通常用σ表示,σ=1/ρ。单位是西门子/米(S/m)。它是描写导体内每点性质的点函数。
电导率
“电阻率”的倒数。
电导率electric conductivity
用以表示电解质溶液导电能力的参数。在电解质的溶液中,带电的离子在电场的影响下产生移动而传递电子,因此,具有导电作用。
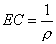
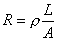
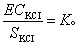 。ECKCl为标准KCl溶液(0.02mol/L)的电导率(mS/cm),18℃时ECKCl=2.397 mS/cm,25℃时为2.765 mS/cm;SKCl为同一电极在相同条件下实际测得的电导度值。那末,待测液测得的电导度乘以电极常数就是待测液的电导率:EC=KS。有些电导仪(如DDS-11A型)有电极常数调节装置,可以直接读出待测液的电导率,无需再用电极常数进行计算。
。ECKCl为标准KCl溶液(0.02mol/L)的电导率(mS/cm),18℃时ECKCl=2.397 mS/cm,25℃时为2.765 mS/cm;SKCl为同一电极在相同条件下实际测得的电导度值。那末,待测液测得的电导度乘以电极常数就是待测液的电导率:EC=KS。有些电导仪(如DDS-11A型)有电极常数调节装置,可以直接读出待测液的电导率,无需再用电极常数进行计算。