亨利定律hengli dinglu
1803年英国化学家W.亨利研究气体在液体中的溶解度时,总结出一条经验规律,“在一定的温度和压力下,一种气体在液体里的溶解度与该气体的平衡压力成正比”。该定律适用的条件是其气体的平衡分压不大,气体在溶液中不与溶剂起作用,(或起一些反应,但极少电离)。被溶解气体的数量可用不同的浓标表示,亨利定律的数学表达式可有下列几种形式:
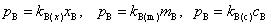
mB——溶质B的质量摩尔浓度,单位为mol·kg-1
cB——为溶质B的物质的量浓度,单位为mol·dm-3
KB(x),KB(m),KB(c)均称为亨利常数,它们的关系是
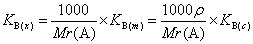
亨利常数也有用单位体积中所溶解气体的体积来表示的。
由于气体溶解在液体中所构成的溶液与其他类型的溶液无区别,故该定律也适应于两种液体组成的稀溶液。
亨利定律
稀溶液定律之一。在一定温度和平衡状态下,气体在液体里的溶解度和该气体的平衡分压成正比。英国化学家亨利(W. Henry,1774—1836)于1803年提出。
- 巴音塔楞沟
- 巴音塔楞额莫内库赛沟
- 巴音布鲁克天鹅保护区
- 巴音布鲁克草原
- 巴音郭勒沟
- 巴音郭楞乌苏河
- 巴音郭楞哈尔萨拉沟
- 巴音郭楞国际旅行社
- 巴音郭楞州泰昌工业总公司
- 巴音郭楞报
- 巴音郭楞石油节
- 巴音郭楞蒙古自治区
- 巴音郭楞蒙古自治州
- 巴音郭楞蒙古自治州主要经济指标
- 巴音郭楞蒙古自治州人民代表大会及其常务委员会
- 巴音郭楞蒙古自治州人民政府
- 巴音郭楞蒙古自治州博斯腾湖流域水环境保护及污染防治条例
- 巴音郭楞蒙古自治州图书馆
- 巴音郭楞蒙古自治州城镇居民最低生活保障
- 巴音郭楞蒙古自治州新科种业有限责任公司尉犁县良种棉轧花厂
- 巴音郭楞蒙古自治州旅游局
- 巴音郭楞蒙古自治州歌舞团
- 巴音郭楞蒙古自治州水资源
- 巴音郭楞蒙古自治州科技协会
- 巴音郭楞蒙古自治州经济开发研究