电解质溶液的依数性dianjiezhi rongye de yishuxing
依数性的函义参见“稀溶液的依数性”。电解质溶液的依数性呈现异常,即稀溶液的渗透压、沸点上升、凝固点降低等值均大于按溶质的分子式所示的分子量的计算值; 反过来说,由实测值计算所得的溶质的分子量小于由其分子式所得的值。例如,对食盐水溶液,其渗透压为
π=iCRT
式中 C——由分子式计算的物质的浓度。
i——校正值,且接近于2
因i首先由J.H.范特荷夫引入,所以把i称做范特荷夫系数,上式称为范特荷夫渗透压公式。由同一浓度的食盐水溶液测定其沸点上升或凝固点降低,得到的i值相同 (均为2) 。
显然,尿素、蔗糖等非电解质溶液的i值应为1。于是得到电解质溶液的依数性为相同浓度的非电解质溶液的i倍。即
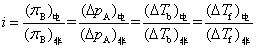
式中 分子——代表电解质溶液的依数性
分母——代表相同浓度下非电解质溶液的依数性
i值——电解质溶液对非电解质溶液的偏差程度。它取决于溶质的本性、溶液的浓度及温度,i值总是大于1。
下图表示在一定温度下,3种盐的水溶液的i值随浓度的变化情况。将这些盐的水溶液无限稀释时,i值各自趋近于2,3和4。
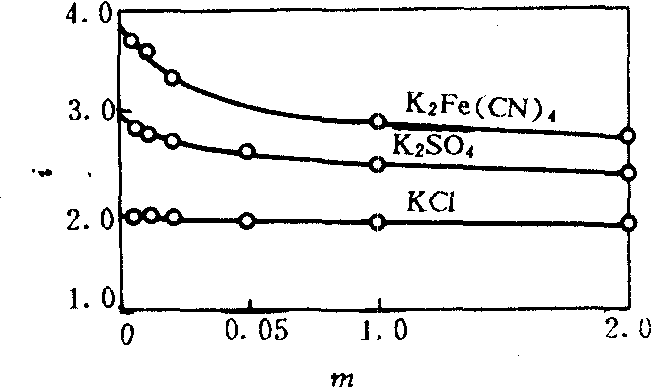
电解质溶液的质量摩尔浓度m与i的关系