米氏方程
表明底物浓度与酶促反应速度间定量关系的公式。从下列假定出发,即1.酶,底物与酶-底物复合物间迅速达成平衡;2.反应速度为起始速度,与酶-底物复合物的浓度成正比,以致从产物逆转成酶-底物复合物的反应可略去不计。可用公式明确表示v=V[S]/(Km+[S]),式中v为反应的起始速度,V为最大速度,[S]为底物浓度,Km为底物常数,也称米氏常数。
米氏方程MichaelisMenten equation
酶促反应中反应速度与底物浓度间相互关系的动力学函数表达式。即v=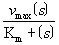 ,其中v为反应速度;vmax为反应最大速度;〔s〕为底物浓度;Km为米氏常数。是酶促反应动力学中的基本公式。在酶浓度和其它条件不变的情况下,当底物浓度较低时,酶促反应速度与底物浓度呈正比,表现为一级反应;当底物浓度很大时,反应速度不再随底物浓度增加而增加,表现为零级反应;当底物处于中间浓度时,表现为混合级反应。米凯利斯(L. Michaelis)和门顿(M.L.Menten)从酶与底物先形成酶底物中间复合物的假说出发,首先推导得此方程,故称之米氏方程。后来,布利格斯(G.E.Briggs)和哈丹尼(J.B.S.Haldane)根据酶底物中间复合物浓度在反应的一段时间内不变(稳态或恒态)的前提下,对此方程作了一些补充和发展。
,其中v为反应速度;vmax为反应最大速度;〔s〕为底物浓度;Km为米氏常数。是酶促反应动力学中的基本公式。在酶浓度和其它条件不变的情况下,当底物浓度较低时,酶促反应速度与底物浓度呈正比,表现为一级反应;当底物浓度很大时,反应速度不再随底物浓度增加而增加,表现为零级反应;当底物处于中间浓度时,表现为混合级反应。米凯利斯(L. Michaelis)和门顿(M.L.Menten)从酶与底物先形成酶底物中间复合物的假说出发,首先推导得此方程,故称之米氏方程。后来,布利格斯(G.E.Briggs)和哈丹尼(J.B.S.Haldane)根据酶底物中间复合物浓度在反应的一段时间内不变(稳态或恒态)的前提下,对此方程作了一些补充和发展。