锑ti
第五周期VA族元素,元素符号Sb。在远古时代,锑就为人们所知,这是由于自然界中辉锑矿Sb2S3比较普遍,而且又容易由辉锑矿制得锑的缘故。在空气中熔烧辉锑矿,它就变成三氧化二锑,再用碳还原就得到锑,锑的名称stibium就取自辉锑矿(stibnite) 的名称。锑一般是以硫化物辉锑矿的形式存在于自然界,锑在地壳中的质量含量比较小,仅为5×10-5%。游离态的晶态锑呈银白色,有金属光泽,但很脆,比一般金属导热导电性都差,但有冷胀性。除了晶态锑外,还有黄锑、灰锑、黑锑等同素异形体,黄锑仅在-90℃以下稳定; 金属变体是锑的稳定形式,其熔点为630.5℃,沸点为1 750℃,相对密度为6.684。2 070℃时锑蒸气为单原子分子。锑是一种不太活泼的元素,与砷有很多相似之处,不同的是锑具有明显的金属性。它仅在赤热时分解水,在室温不会被空气氧化,但能与氟、氯、溴化合; 加热时才能与碘和其他非金属化合,它易溶于热硝酸,形成水合的氧化锑,能与热浓硫酸反应,生成硫酸锑,也能与强碱形成亚锑酸盐。锑常呈+Ⅲ和+Ⅴ氧化态。锑能形成许多剧毒的化合物,如锑烟。锑化氢SbH3是毒气,与胂生成条件相同,加热时比胂更易分解。锑和金属形成的锑化物可看做是金属原子取代锑化氢中的氢的生成物。一些锑化物,如锑化铝、锑化镓和锑化铟,具有半导体性,用于电子工业。三氧化二锑是典型的两性化合物,碱性略占优势,在强酸中溶解生成锑 (Ⅲ) 盐:
Sb2O3+3H2SO4=Sb2(SO4)3+3H2O
也溶于碱,生成亚锑酸盐或偏亚锑盐,如:
Sb2O3+2NaOH=2NaSbO2+3H2O
SbCl3+3NaOH=Sb(OH) 3↓+3NaCl
沉淀易溶于过量碱或酸中。锑 (Ⅲ) 盐作为弱碱盐,水溶液中水解而生成碱式盐: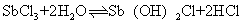
Sb (OH) 2Cl=SbOCl↓+H2O
氯化氧锑中的SbO+称为锑酰或氧锑离子。五氧化二锑主要呈酸性,是锑酸的酐,锑酸在水溶液中有好几种存在形式,其盐为锑酸盐。桔红色的三硫化二锑性质上类似于硫化砷,溶解于碱金属和铵的硫化物中生成硫代酸盐。锑主要用做硬铅添加剂以及用于制造金属轴承、焊剂和铅字合金、锑盐和颜料等。超纯锑的金属化合物是重要的半导体及红外探测器材料。在古代,古希腊人用“硫化锑矿”做描眉的黑色颜料,硫化锑还用于火柴生产和橡胶工业,此外还有用途颇广的锑白及各种医用锑等。可将辉锑矿与铁屑混合共热而取代出锑,或煅烧成氧化物后再与碳共热来还原出锑。锑
银白色重金属。在地壳中的含量仅为0.000005%。元素符号为Sb,原子量为121.75,密度为6.68g/cm3。锑的性质是质硬而脆,没有延展性,为不良导体(其导电率仅为银的4.2%),但有较好的化学稳定性,在空气中不会被氧化,可生成多种氧化物。锑早在远古时代就得到了应用,人们多用其生产青铜。进入20世纪以来,世界锑工业得到了适度发展。20世纪末,世界锑消费量已超过了15万 t。锑的主要用途是配制各种合金,如制作蓄电池铅锑合金板、轴承合金、焊锡、电缆包皮、耐磨元件及各种硬铅产品等。这方面耗锑量约占锑消费总量的50%左右。此外,锑的氧化物还被用于搪瓷、化纤、玻璃等行业,还能用于制作颜料、涂料 、油漆和阻燃剂等产品。高纯锑则可作硅、锗半导体材料的掺杂元素。中国是世界上最大的产锑国,也是锑产品的最大出口国。2000年,中国共出口锑产品8.36万 t,约占世界锑产品出口量的80%。