不同浓度酸或碱混合后的pH值计算butongnongdu suan hou jian hunhehou de pHzhi jis-uan
不同浓度同种酸或碱混合时,一般因浓度较小时,混合液的体积可认为是混合前各溶液体积之和(如果给出溶液密度,则应通过密度求混合液之体积)。溶质的量是各溶液溶质量的总和,算出混合液的H+浓度,即可算其pH值。强电解质溶液混合时,可直接计算其H+浓度。弱电解质溶液混合时必须考虑浓度变化对电离平衡的影响,用电离常数、电离度和浓度来计算H+,然后求pH值。
例1 10mL pH1=2的盐酸溶液与20mL pH2=3的盐酸溶液混合,求混合液的pH3值。解 盐酸为强电解质,pH1=2,所以
〔H+〕1=0.01mol·L-1;
pH2=3,〔H+〕2=0.001mol·L-1混合后:
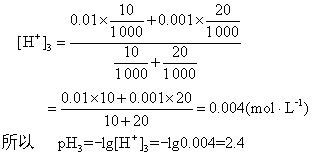
答 混合液的pH为2.4。
例2 pH1=12和pH2=10的氢氧化钠溶液各100mL混合,求混合液的pH3值。
解 NaOH为强电解质在水中100%电离

答 混合液的pH为11.7。
例3 0.1mol·L-1醋酸溶液100mL与0.01mol·L-1醋酸溶液200mL相混合,求混合液的pH值(已知醋酸的电离常数为1.8×10-5)。
解 混合液的浓度
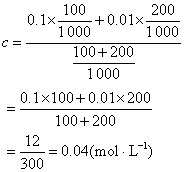
平衡时H+浓度为x,根据方程:
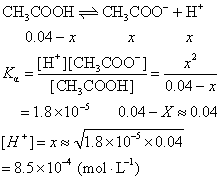
pH=-1g〔H+〕 =-1g8.5×10-4=3.07
答 混合液的pH为3.07。